Построение систематических курсов химии VIII класса для формирования понятия о химической реакции
Среди подобных отечественных курсов можно рассмотреть учебник О.С.Зайцева. Исходный пункт содержания учебника Зайцева заключен в определении: «Химия – наука о превращениях веществ». Курс практически представляет собой последовательное изучение важнейших теорий, начинающееся с учения о периодичности и строении вещества. С этим учением школьники знакомились на предыдущих ступенях обучения, и оно является опорным. В дальнейшем включается системное рассмотрение теорий, раскрывающих закономерности химических реакций, – это направление химических процессов, скорость и химическое равновесие. Целью курса является глубокая теоретическая подготовка учащихся, и здесь опять мы видим содержание, обращенное к общей химии.
Во всех случаях следует иметь в виду, что содержание школьного курса химии, в том числе и профильного, не должно сводиться к переносу в школу вузовского курса химии. На данном этапе мыслительный аппарат школьника еще недостаточно сформирован и к такому варианту не подготовлен. Кроме того, выбор содержания зависит от условий работы школы, особенностей контингента учащихся и некоторых других факторов, определяемых социальным заказом общества.
На основании прочитанного попробуйте проверить себя, свое понимание.
Задания
1. Докажите, что курс органической химии в средней школе построен с ориентацией на формирование и развитие системы понятий о веществе.
Примерный ответ. Kурс органической химии изучается последовательно от углеводородов к кислородсодержащим и к азотсодержащим органическим веществам, в том числе и к жизненно важным: жирам, углеводам и белкам. При этом прослеживается изменение в строении углеродного скелета и усложнение строения функциональных групп. Химические реакции отражают свойства этих веществ в зависимости от их состава и строения. Из этого можно заключить, что курс органической химии ориентирован на формирование и развитие системы понятий о веществе.
2. Постарайтесь раскрыть последовательность формирования каждого блока понятий о химическом элементе на примере реализуемого вами курса химии.
Примерный ответ. Система понятий о химическом элементе включает три блока: атомы химических элементов, классификация химических элементов и круговорот элементов в природе.
Сначала атом химического элемента рассматривается как химически неделимая частица, имеющая массу, затем изучается внутриатомное строение. Классификация химических элементов вначале ограничивается делением на металлы и неметаллы, затем выделяются элементы с двойственными свойствами, и в завершение следует изучение периодического закона и периодической системы элементов Д.И.Менделеева. Периодическая система – это высшее обобщение знаний о химических элементах. Распространенность элементов в природе и их круговорот раскрываются по мере изучения соответствующих им простых веществ.
3. Используя приведенный выше перечень компонентов системы понятий о химической реакции, по образцу схемы 4 постройте схему системы понятий о химической реакции.
Примерный ответ.
Структура системы понятий о химической реакции
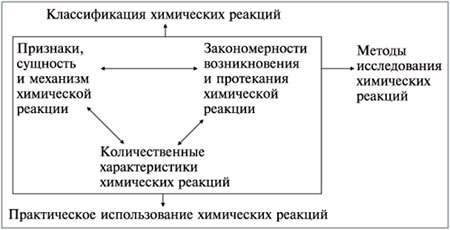
Рис.
4. Рассмотрите таблицу «Kлассификация химических реакций» (см. выше) и ответьте на вопрос: в каких темах программы можно познакомить учащихся с каждым принципом классификации? Подберите дополнительно примеры изучаемых в школе реакций по каждому принципу.
Примерный ответ.
Гомогенные реакции – окисление оксида азота(II) кислородом:
2NO + O2 = 2NO2 (тема «Азот»)
и взаимодействие водорода с хлором:
Н2 + Сl2 = 2HCl (тема «Галогены»).
Гетерогенная реакция – взаимодействие оксида серы(IV) с водой:
SO2 + H2O ![]() H2SO3 (тема «Сера»).
H2SO3 (тема «Сера»).
Окислительно-восстановительные реакции – горение магния в кислороде:
2Mg + О2 = 2MgO (тема «Первоначальные химические понятия»),
горение аммиака в кислороде:
4NH3 + 3O2 = 2N2 + 6H2O (тема «Азот»),
восстановление оксида меди водородом:
СuO + H2 = Cu + H2O (тема «Водород, кислоты, соли»).
(Названия тем могут быть и другие, в зависимости от того, какими учебниками вы пользуетесь.)
Реакции, где окислительно-восстановительный процесс отсутствует, – взаимодействие нитрата серебра с хлоридом натрия:
Разработка примерного творческого проекта «Эйфелева башня»
При рассмотрении всех выше предложенных изделий можно сделать вывод: для методического обеспечения элективного курса «Компьютерное моделирование и изготовление изделий на станках с ЧПУ» лучше всего выбрать изделие с пазловым соединением. Подобные соединения требуют от учащегося при составлении комп ...
Особенности подготовительной работы над написанием изложений
В начальных классах национальной школы изложение проводится по изученному и усвоенному, прочитанному в классе небольшому тексту. Как обучающее можно проводить изложение с открытым текстом. Письменному изложению должна предшествовать большая подготовительная работа. Материал для изложения должен быт ...
Характеристика базы исследования навыка чтения в
СОШ с. Новоманошкино
Чтение — это сложный комплексный вид деятельности, состоящий из ряда операций. Достаточно полно навык чтения может характеризовать совокупность нескольких его параметров: способ, скорость, правильность, автоматизированность (так называемая «беглость») и понимание прочитанного [16, с. 140]. Актуальн ...
Навигация
- Главная
- Воспитание детей в семье
- Теория воспитания
- Формы обучения в высшей школе
- Идея построения адаптивной школы
- Половое воспитание
- Специальная педагогика
- Развитие образования

